كيمياء الحياة
كان يُعتقَد فيما مضى أن إنتاج المركبات العضوية يقتصِر على الكائنات الحية وأنه لا يمكن تخليقها في المعمل. ومع أنه تبيَّن لنا حاليًّا أن الأمر ليس كذلك، فمن الواضح أن الجزيئات العضوية ضرورية لوجود حياة على هذا الكوكب. شرحنا في الفصل الثالث كيف يجري علماء الكيمياء العضوية عمليات تخليق الجزيئات العضوية من مواد أولية جزيئية أصغر. قد تبدو هذه العملية غايةً في البراعة، إلا أن الطبيعة كانت — ولا تزال — تفعل الأمر نفسه منذ أمدٍ بعيد، بل وبكفاءةٍ أعلى بكثير. فمن مواد أولية جزيئية بسيطة للغاية، أوجدت الحياة تنوُّعًا مذهلًا من الجزيئات، بعضها ذات بُنًى شديدة التعقيد من الصعب للغاية تخليقُها في المعمل. لا تنتج الحياة جزيئات مُعقدة فحسب، بل تفعل ذلك في وسطٍ مائي في ظلِّ ظروفٍ معتدلة غير متطرفة.
الأحماض الأمينية والبروتينات



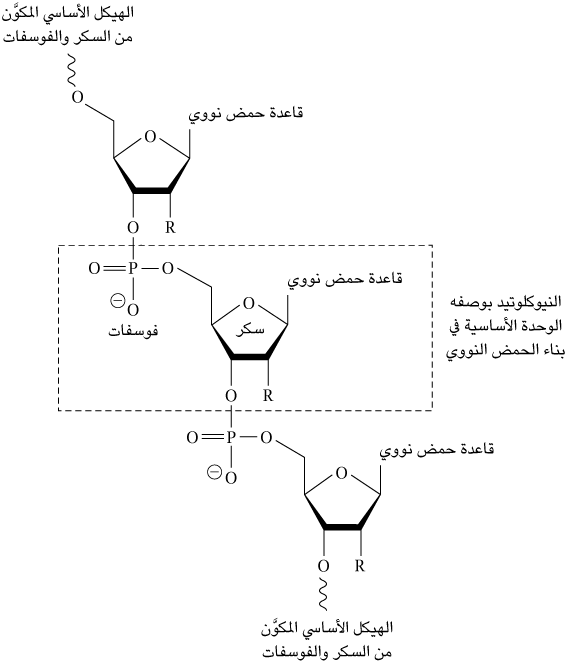
النيوكليوتيدات والأحماض النووية



المزيد من عمليات التخليق الحيوي

وظيفة البروتينات



إن حالة التوافق المُستحَث ضرورية لعمل الآلية التي يستخدمها المُستقبِل في توصيل الرسائل إلى داخل الخلية، وهي العملية التي تُسمَّى نقل الإشارة. وبتغير شكل البروتين، يبدأ سلسلة من الأحداث الجزيئية التي تؤثر في الكيمياء الداخلية للخلية. على سبيل المثال، بعض المستقبلات تكون جزءًا من مركبات متعددة البروتينات تُسمى القنوات الأيونية. عندما يُغيِّر البروتين المستقبِل شكلَه، فإنه يجعل القناة الأيونية بأكملها تُغير شكلها. ويؤدي هذا إلى إحداث فتحة مركزية تسمح بتدفُّق الأيونات عبر جدار الخلية. وبذلك، يتغيَّر تركيز الأيونات داخل الخلية، الأمر الذي يؤثر بدوره في التفاعُلات الكيميائية التي تتم داخلها، وهو ما يؤدي في نهاية المطاف إلى نتائج ملحوظة مثل انقباض العضلات. لا تكون جميع المستقبلات مرتبطةً بجدار الخلية. على سبيل المثال، توجَد مستقبلات الأستيرويد داخل الخلية. يعني ذلك أن الهرمونات الأستيرويدية تحتاج إلى النفاذ عبر الجدار الخلوي لكي تصِل إلى المُستقبِلات المستهدَفة.
توجد البروتينات الناقلة أيضًا مدمجةً في جدار الخلية، وهذه البروتينات هي المسئولة عن نقل جزيئاتٍ قطبية مثل الأحماض الأمينية إلى داخل الخلية. كما أنها مهمة للتحكم في نشاط الأعصاب حيث تتيح للأعصاب اقتناص الناقلات العصبية المُطلَقة، بحيث يستمر نشاطها لفترة محدودة فقط. تحتوي البروتينات الناقلة على مواضع ارتباط خارج الخلية، ترتبط بالجزيئات المستهدَفة. بمجرد حدوث هذا الارتباط، يمر الجزيء عبر البروتين وينطلق إلى داخل الخلية.
وظيفة الأحماض النووية
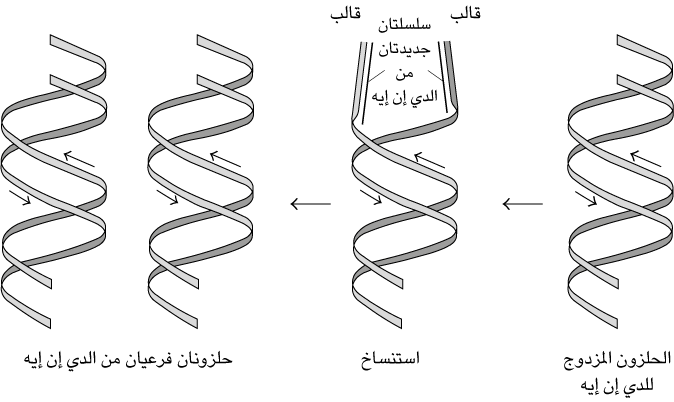
الحمض النووي الريبوزي (آر إن إيه)، على الجانب الآخر، هو نوع آخر من الأحماض النووية الموجودة في الخلايا، وهو ضروري لعملية تخليق البروتينات (عملية الترجمة). توجد ثلاثة أنواع من الحمض النووي الريبوزي: الحمض النووي الريبوزي المرسال (إم آر إن إيه)، والحمض النووي الريبوزي الناقل (تي آر إن إيه)، والحمض النووي الريبوزي الريبوسومي (آر آر إن إيه). يحمل الحمض النووي الريبوزي المرسال الشفرة الوراثية لبروتين مُعين من الدي إن إيه إلى موضع إنتاج البروتين. وعادةً ما يكون هذا النوع نسخةً من شريطٍ واحد لجزءٍ مُعين من الدي إن إيه. تُسمى عملية نسخ هذه المعلومات بعملية النسخ.
يفكُّ الحمض النووي الريبوزي الناقل الشفرةَ الثلاثية المحمولة على الحمض النووي الريبوزي المرسال من خلال العمل بمثابةِ مُحوِّل جزيئي. توجَد مجموعة مكوَّنة من ثلاث قواعد (مضاد الرامزة) عند أحد طرفَي الحمض النووي الريبوزي الناقل، والتي يُمكنها الارتباط بثلاث قواعد على الحمض النووي الريبوزي المرسال (الرامزة). يرتبط حمض أميني مع الطرف الآخر للحمض النووي الريبوزي الناقل، ويعتمِد نوع هذا الحمض النووي على مضاد الرامزة الموجود. عندما ترتبط قاعدة مضاد الرامزة المناسبة على الحمض النووي الريبوزي الناقل مع الرامزة على الحمض النووي الريبوزي المرسال، فإنه يحضر معه الحمض الأميني الذي شفَّرته هذه الرامزة.

التطور الكيميائي
في ثمانينيات القرن التاسع عشر، اقترحَ تشارلز داروين أنَّ المواد الكيميائية العضوية الضرورية للحياة ربما نشأت في «بركة صغيرة دافئة». ومنذ ذلك الحين، ظل علماء الكيمياء العضوية يضعون فرضياتٍ تتعلَّق بكيفية تكوُّن وحدات البناء الأساسية الضرورية للحياة على كوكب الأرض على مدار المليار عام التي سبقت نشأة الحياة على الكوكب. يُعرف هذا الموضوع باسم التطوُّر الكيميائي أو الكيمياء ما قبل الحيوية.
كان من أوائل علماء الكيمياء الذين درسوا التطوُّر الكيميائي ستانلي إل ميلر وهارولد سي يوري في جامعة شيكاجو. في عام ١٩٥٣، أجرَيا تجربةً صُمِّمت لمحاكاة الظروف البيئية التي ربما كانت موجودة خلال الحقبة ما قبل الحيوية. واقترحا أن الغلاف الجوي للأرض كان يحتوي في البداية على غازاتٍ مثل الميثان والأمونيا بدلًا من الأكسجين، حيث لم يظهر الأكسجين في الغلاف الجوي إلا بعد ظهور الحياة النباتية.
تضمَّنت التجربة التي أعدَّها ميلر ويوري دَوْرقًا مستديرَ القاعدة يحتوي على ماء لمحاكاة المحيطات، وخليطًا من الميثان والأمونيا والهيدروجين لتمثيل الغلاف الجوي. وُضِعَ قطبان كهربيان في داخل الدورق ومُرِّرت عبرهما شحناتٌ كهربية لمحاكاة البَرْق. كان المقترَح أن البرق يُمكنه توفير الطاقة المطلوبة لتحفيز التفاعُلات بين الجزيئات الغازية، وأن نواتج هذه التفاعلات سينتهي بها المطاف بالذوبان في مياه «المحيط».
استغرقَ إجراءُ التجربة أسبوعًا كاملًا، وعند تحليل الماء، اكتُشِف وجود عدد من الأحماض الأمينية التي تكوَّنت طبيعيًّا. أقنعت هذه التجربة وحدَها الكثير من العلماء بأنه من المُمكن خلق الحياة، ليس على الأرض فحسب، بل أيضًا في أي مكانٍ آخر في الكون.

تُوجد نظرية أخرى في التطوُّر الكيميائي مفادها أنَّ وحدات البناء الأساسية التي تشكَّلت منها الحياة قد نشأت في فوهاتٍ مائية حرارية في أعماق البحار. أطلقت هذه الفوهات خلائط المركبات الكيميائية اللازمة لحدوث التفاعُلات قبل الحيوية، كما وفَّرت الحرارة كمصدر للطاقة. علاوةً على ما سبق، تحقَّقت الحماية اللازمة للنواتج المُتكوِّنة من البيئة العدائية التي كانت سائدة على سطح الكوكب في ذلك العصر، الأمر الذي منحها فرصة أكبر لتكوين البوليمرات الحيوية مثل البروتينات والأحماض النووية.
تقترح نظريةٌ أخرى أن وحدات الحياة الأساسية قد خُلِّقت في الفضاء الخارجي، ثم جُلِبَت إلى الأرض مع سقوط الشهب والنيازك. تختصُّ الكيمياء الفلكية، وهي أحد فروع الكيمياء، بدراسة هذه الاحتمالية عن طريق البحث عن جزيئاتٍ عضوية غير أرضية. على سبيل المثال، اتضح أن الميثان هو المكوِّن الرئيسي في الغلاف الجوي لكلٍّ من المُشتري وزُحل وأورانوس ونبتون. تبحث مركبة «كيوريوسيتي روفر» التابعة إلى وكالة ناسا عن الجزيئات العضوية على سطح المريخ، وفي نوفمبر عام ٢٠١٤، أطلق مسبار «روزيتا» التابع إلى وكالة الفضاء الأوروبية كاشفًا روبوتيًّا يُدعى «فايلاي» للهبوط على سطح أحد النيازك. وقد كشفت البيانات الأولية عن وجود جزيئاتٍ عضوية في الغلاف الجوي للنيزك. كما يهتم العلماء باكتشاف إذا ما كانت هناك جزيئاتٌ عضوية في الغلاف الجوي للقمر تيتان (أحد أقمار كوكب زُحل). يدور مسبار «كاسيني» في مدار حول هذا القمر منذ عام ٢٠٠٤، ومن المعروف حاليًّا أن القمر تيتان له غلاف جوي يحتوي على هيدروكربونات عطرية مُتعددة الحلقات. ومِن المُحتمَل أيضًا أن تتضمَّن بحيرات الميثان على القمر تيتان جزيئاتٍ عضوية تحتوي على النيتروجين. ولكن نظرًا إلى قلة الأكسجين والانخفاض الشديد لدرجات الحرارة على سطح القمر تيتان، فلا يوجد احتمالٌ يرجِّح تطوُّر أي شكلٍ من أشكال الحياة على سطحه.
أما على سطح الأرض، فقد أُجري العديد من التجارب لمحاكاة الظروف في الفضاء الخارجي والتعرُّف على تفاعُلات التخليق التي يمكن أن تحدُث. وكان من بين الاحتمالات المطروحة أن التفاعلات تحدث على النيازك نتيجة الرياح الشمسية التي تؤثر في الفورماميد؛ وهو جزيءٌ عضوي بسيط اكتُشِفَ بكمياتٍ كبيرة في الفضاء. نتجَت عن تجارب المحاكاة، التي أُسقط خلالها شعاعٌ بروتوني على خليطٍ من الفورماميد وغبار النيزك، مجموعة متنوعة من الوحدات الجزيئية الأساسية للحياة. ثمة اهتمام خاص بمجموعة من النيازك، تُسمَّى الكوندريتات. وهي أقدم النيازك الموجودة في الفضاء، ويُعتقَد أنها قد تساعد في تحفيز التفاعُلات. إذا ما «لقَّحت» هذه النيازك الكواكب بالوحدات الكيميائية الأساسية اللازمة لنشأة الحياة، فمن المتوقَّع أن تتشابه الحياةُ المحتمَل اكتشافها في أي مكانٍ من الكون مع الحياة على الأرض، ويكون هذا التشابُه على المستوى الجزيئي. الاعتراض الوحيد على نظرية «تلقيح» النيازك هي الفصل في قدرة الجزيئات العضوية على النجاة من الحرارة الشديدة الناتجة عن اختراق النيزك للغلاف الجوي للكوكب من عدمها.
أحد الألغاز المرتبطة بالتطوُّر الكيميائي كيفية انتقاء الأيزومرات الضوئية المفردة للأحماض الأمينية والكربوهيدرات بوصفِها الوحدات الأساسية المُفضَّلة لإنشاء البروتينات والأحماض الأمينية. توجد نظرية تُسمى «فرضية فيستر وأولبريخت»، تستند إلى حقيقة أن الإلكترونات تدور يمينًا ويسارًا. يؤدي الإشعاع المُستقطَب، الذي يتكوَّن إما من إلكتروناتٍ تدور ناحية اليسار فقط وإما من إلكتروناتٍ تدور ناحية اليمين فقط، إلى انحلال أحد الأيزومرَين الضوئيَّين لجزيءٍ كيرالي بسرعة أكبر من انحلال الأيزومر الآخر. توجد بعض الأدلة التجريبية على ذلك. ولكنها لا تزال بحاجةٍ إلى إثبات صحتها في كلٍّ من الأحماض الأمينية والكربوهيدرات.
تطوُّر البوليمرات الحيوية اللازمة لنشأة الحياة
يمكن أن تتكوَّن الأحماض الأمينية والكربوهيدرات والأحماض النووية في ظل مجموعة متنوعة من الظروف البيئية في الحقبة ما قبل الحيوية، ولكنها لا تستطيع أن تتبلمر لتكوين البروتينات أو الأحماض الأمينية. لكي تحدث عملية البلمرة، لا بدَّ من وجود عامل حفَّاز. في الخلايا الحية، يُحفَّز تخليقُ الدي إن إيه بواسطة البروتينات، ولكن تخليق هذه البروتينات يعتمد على المعلومات الوراثية المخزَّنة في الدي إن إيه نفسه. ومن ثَمَّ، فإن كلًّا من عمليتَي التخليق تعتمِد على الأخرى. علاوة على ذلك، تعتمِد الحياة على المعلومات الوراثية التي تنتقل من جيلٍ إلى آخر. ومن ثَمَّ، فالسؤال هنا: كيف تطوَّرت الحياة؟
تقترح إحدى النظريات أن هناك جزيئًا قد تكوَّن في ظروف الحقبة ما قبل الحيوية التي ربما حفَّزت استنساخه لنفسه. وثمة نقاشٌ حول ماهية هذا الجزيء، وما إذا كان شكلًا مبكرًا من البروتينات أو بِنية دي إن إيه. ولكن ثمة مشكلات تتعلَّق بكلا الاحتمالَين. من المعروف أن الأحماض الأمينية ترتبِط معًا لتكوِّن ببتيدات في وجود عاملٍ حفَّاز بسيط يُسمَّى السياناميد، الذي يمكن أن يتكوَّن من تفاعُل الميثان والأمونيا في ظروف الحقبة ما قبل الحيوية. ولكن لا يمكن التحكم في تسلسُل ارتباط الأحماض الأمينية معًا، أو في الآلية المُستخدَمة في نسخ الببتيدات المفيدة.
فيما يتعلق بالدي إن إيه، يمكن أن تتكوَّن سلاسل حمض نووي صغيرة تُسمى قليلات النيوكليوتيد في ظروف الحقبة ما قبل الحيوية. وتكون لهذه الجزيئات القدرة على العمل بمثابة قوالب لنسخ جزيئاتٍ مُتطابقة، ولكنها تكون قصيرة للغاية ولا يُمكنها تخزين معلوماتٍ وراثية مفيدة، ولا تُوجَد أيُّ آلية تحفيز من الحقبة ما قبل الحيوية يُمكنها تحفيز استنساخها.
يعتقد أغلبُ العلماء حاليًّا أن الجزيء الرئيسي الذي أطلق شرارة تطوُّر الحياة هو الحمض النووي الريبوزي (آر إن إيه). وهذا اقتراحٌ معقول إذا ما وضعنا في الاعتبار الدور المحوري الذي يلعبه الآر إن إيه حاليًّا في تخليق البروتينات. ربما تطوَّر نوعٌ مبكر من الآر إن إيه وأصبح بمثابة قالبٍ لتخليق نُسَخ متطابقة، وفي هذه الحالة ربما كان الآر إن إيه سيُصبح جزيء التخزين الأصلي للمعلومات الوراثية. من بين الفرضيات الأخرى أيضًا أن هذا النوع المُبكر من الآر إن إيه ربما حفَّز عملية استنساخٍ ذاتي. أثبتت الأبحاثُ الحديثة أن بعض جزيئات الآر إن إيه الحالي لها بالفعل خصائص تحفيزية. تُسمَّى هذه الجزيئات الريبوزيمات. وربما اعتمدت صور الحياة المبكرة على الريبوزيمات لتأدية الوظائف التي يؤديها حاليًّا الحمض النووي الريبوزي المنقوص الأكسجين والبروتينات. وكان من بين الاقتراحات أيضًا أن الريبوسومات في الخلايا الحالية ربما تطوَّرت من أحد الريبوزيمات المبكرة. وتكون المناطق المركزية في ريبوسومات الكائنات المُختلفة متماثلةً نسبيًّا، الأمر الذي قد يُوحي بوجود سلَف جزيئي مشترك منذ ٣٫٨ مليار سنة مضت. ولعلَّ هذا السلف المشترك كان السِّمة الأساسية التي ميَّزت التحوُّل الجذري من الكيمياء قبل الحيوية إلى نشأة الحياة نفسها.
الاستفادة بالبروتينات والأحماض النووية
يتزايد استخدام الإنزيمات والأحماض النووية في التطبيقات التجارية. على سبيل المثال، تُستخدَم الإنزيمات عادةً في تحفيز التفاعلات التي تُجرى في معامل الأبحاث، وفي العديد من العمليات الصناعية المُتعلقة بمجالاتٍ مثل المستحضرات الدوائية والكيماويات الزراعية والوقود الحيوي. كانت الإنزيمات تُستخرَج فيما مضى من مصادر طبيعية، وكانت هذه العملية مكلِّفة وبطيئة. ولكن، يمكن للهندسة الوراثية حاليًّا إدخال الجين الخاص بأيٍّ من الإنزيمات الأساسية في الدي إن إيه الخاص بخلايا جرثومية سريعة النمو، مما يسمح بالحصول على الإنزيمات بسرعة أكبر وبكمياتٍ أوفر بكثير. أتاحت الهندسة الوراثية أيضًا إمكانية تعديل الأحماض الأمينية لتخليق أيٍّ من الإنزيمات. قد تكون هذه الإنزيمات المعدَّلة أكثر فاعليةً كعوامل حفَّازة، وتقبل عددًا أكبر من الركائز، وتصمد في ظروف التفاعُل الأصعب. على سبيل المثال، استُخدِم إنزيم معدَّل لتحفيز خطوةٍ مهمة في عملية تخليق السيتاجليبتين، وهو مادة تُستخدَم في علاج مرض السكري. لم يتمكَّن الإنزيم الطبيعي من تحفيز هذا التفاعُل لأن الركيزة المشاركة في التفاعل كانت أكبر من الموضع النشط بكثير. وبذلك، نجحت الهندسة الوراثية في إنتاج إنزيمٍ معدَّل يتضمَّن موضعًا نشطًا أكبر.
تعمل شركاتٌ مثل «نوفوزيم» و«دو بونت» في مجال تصميم الإنزيمات المعدَّلة. على سبيل المثال، تحتوي مساحيق الغسيل الحيوية على مجموعةٍ متنوعة من الإنزيمات التي تحفِّز إزالة بقع الطعام أو الدم أو العرق الصعبة. ذلك حيث يكسِّر البروتياز الروابط الببتيدية في البروتينات، ويكسِّر الليباز مجموعة الإستر في الليبيدات والدهون، ويحلل الأميلاز النشويات. يحلِّل السليولاز ألياف السليلوز في الملابس جزئيًّا للمساعدة في تحرير جسيمات الأوساخ العالقة بها.
لا تزال تُكتشَف إنزيماتٌ جديدة في الطبيعة، وكذلك في المعامل. فالفطريات والبكتيريا غنية جدًّا بالإنزيمات التي تُمكِّنها من تحليل المركبات العضوية. ووفقًا للتقديرات، فإن الخلية البكتيرية العادية تحتوي على نحو ٣ آلاف إنزيم، بينما تحتوي الخلية الفطرية على ٦ آلاف إنزيم. وبالنظر إلى الأنواع العديدة الموجودة من البكتيريا والفطريات، فإنها تُمثل مستودعًا هائلًا للإنزيمات الجديدة، وحسب التقديرات لم يُدرَس سوى ٣٪ فقط من هذه الأنواع حتى الآن. علاوةً على ذلك، يمكن أن تشكِّل الكائناتُ الدقيقة، التي لا تتأثر بالظروف المناخية الشديدة التطرف، أهمية كبيرة للغاية في إنتاج إنزيماتٍ يُمكنها العمل في ظل الظروف القاسية. على سبيل المثال، تُفرز الكائنات الدقيقة التي يُمكنها العيش في القطب الشمالي إنزيماتٍ تفاعلية في درجة حرارة الغرفة ولا يلزم فيها تحفيز التفاعُلات عن طريق التسخين. على سبيل المثال، اكتُشِفَ البروتياز الذي يُمكنه العمل في درجات الحموضة العالية من كائناتٍ دقيقة تنمو في المقابر. واتضحَ أن هذا الإنزيم إضافة مُفيدة في مجال المنظِّفات.
اتضحت أهمية استخدام بعض الإنزيمات، بما فيها الأميلاز، في إنتاج الوقود الحيوي مثل الإيثانول. تُحفِّز هذه الإنزيمات تَحلُّل النشا والجليكوجين الموجودَين في قصب السكر والذرة الصفراء. ولكن للأسف، يُوجَد الكثير من العقبات التي تعترض إنتاج الوقود الحيوي من المحاصيل الغذائية؛ لأن هذا من شأنه أن يُقلِّل كميات المواد الغذائية في المتاجر ويؤدي بالتالي إلى ارتفاع أسعارها. تُوجَد طريقة أفضل وهي استغلال المواد النباتية المُهدرة حاليًّا. في سبيل ذلك، تُجرى أبحاث حاليًّا للحصول على إنزيمات السليولاز التي تفكِّك السليلوز الموجود في أوراق النباتات وسيقانها. على سبيل المثال، أنتجت شركة «نوفوزيم» خليطًا من إنزيمات السليولاز يُسمَّى «سيليك»، ويمكن استخدامه في إنتاج الإيثانول الحيوي.
مِن المتوقَّع أن تثبت الإنزيمات أهميتها أيضًا في توفير الكثير من الكواشف والمواد الكيميائية التي يُعَدُّ النفط مصدر الحصول عليها حاليًّا. على سبيل المثال، يلزم إنتاج ٥٫٥ ملايين طن كلَّ عامٍ من حمض الأديبيك؛ وهو مكوِّن أساسي مطلوب في تخليق النَّيْلون. كان النفط هو المصدر المعتاد لحمض الأديبيك في الماضي، ولكن من المتوقَّع أن يقلَّ إنتاج النفط التقليدي بما يزيد على ٥٠٪ على مدار العقدَين القادمَين، ولا يصلح أسلوب التصدُّع المائي (التكسر الهيدروليكي) لأنْ يكون حلًّا طويل الأمد. ومن المتوقَّع أن تلعب الإنزيمات دورًا محوريًّا في إنتاج هذه المواد الكيميائية المهمة من مصادر بديلة.
توجد بعض التطبيقات غير المعتادة للإنزيمات. على سبيل المثال، تُجرى أبحاث الآن للكشف عن إمكانية استخدام الإنزيمات كمكوناتٍ في البطاريات. تدور الفكرة حول ربط الإنزيمات بأقطاب كهربية، واستخدام الجلوكوز كوقود. تُحفِّز الإنزيمات أكسدة الجلوكوز، مما يؤدي إلى توليد إلكتروناتٍ تُنقَل إلى القطب الكهربي. من المتوقَّع أن تُصبح هذه البطاريات، في نهاية المطاف، مصدرًا للطاقة في الهواتف المحمولة، وناظمات القلب، وغيرها من الأجهزة الصغيرة.
يوجد بعضُ التطبيقات المحتمَلة لأنواع أخرى من البروتينات. على سبيل المثال، هناك بروتين يُسمَّى «رفليكتين» هو المسئول بدرجة كبيرة عن أسلوب التخفِّي الذي يستخدمه كلٌّ من الحبَّار والأخطبوط والسُّبيط. في حال فسفرة البروتين، يحفِّز هذا البروتين خلايا تُسمى حاملة الصبغة لعكس الضوء، بحيث يعكس الكائن صورة مُحيطه. ويدرس العلماء حاليًّا إمكانية استخدام عمليةٍ مماثلة في تصميم مواد تَخفٍّ جديدة. كما تُجرى الآن تجارب لمعرفة إذا ما كانت المواد القائمة على هذه التقنية يُمكنها أن تعكس الحرارة كذلك. وسيكون نجاح هذه التجارب إيذانًا بإمكانية تصميم ملابس ذكية قادرة على تنظيم كمية الحرارة التي ينبغي إطلاقها إلى البيئة المُحيطة حتى يكون المعطف باردًا في الأيام الدافئة ودافئًا في الأيام الباردة.
تدرس الآن العديدُ من الفِرق العلمية البروتينات التي تتيح للكائنات الحية العيش في الأجواء الشديدة البرودة. على سبيل المثال، يمكن ليرقات خنافس ألاسكا أن تعيش في درجات حرارة شديدة الانخفاض تصل إلى ١٠٠ درجة تحت الصفر. واكتُشِفَ أن بعض البروتينات يُمكنها أن تعمل كمضادَّات تجمُّد طبيعية تحُول دون تكوُّن بلورات الثلج داخل الخلايا. ذلك حيث «تُجفِّف» بنية البروتين بلورات الثلج الدقيقة وتجعلها لا تزيد في الحجم. ثمة استخداماتٌ تجارية مُحتملة للبروتينات التي تعمل بهذه الطريقة. وفعليًّا، تُستخدَم الآن البروتينات المضادة للتجمُّد في صناعة الآيس كريم؛ لأنها تحدُّ من حجم بلورات الثلج المُتكوِّنة. وهذا يجعله ذا ملمسٍ ناعم ويسمح بإزالة المحتوى الدهني منه.
تتضمَّن الاستخدامات التجارية الأخرى للدي إن إيه عددًا من الأجهزة التشخيصية التي يمكنها الكشف عن الفلزات الموجودة في الماء، والغازات السامة، والطعام الفاسد، والفيروس المسئول عن مرض الإيبولا. كما يوجد استخدام آخر مُحتمَل وهو استخدام الدي إن إيه كقالب لتخليق البوليمرات. أثبتت التجارب أن الدي إن إيه يمكنه الارتباط بمحوِّلات جزيئية تحمل المونومرات اللازمة لتخليق البوليمرات. بمجرد أن ترتبط المحولات الجزيئية بقالب الدي إن إيه، تحدث عملية البلمرة وينطلق البوليمر. استُخدِمت هذه الطريقة من قبل في إعداد البولي إيثيلين جليكول.
كذلك اكتُشِفَ أن الدي إن إيه المستخرَج من الحيوانات المنوية لأسماك الرنجة يمكن أن يُستخدَم كعامل لإخماد الحرائق. عندما ينحلُّ الدي إن إيه بفِعل النيران، ينطلق غاز الأمونيا الذي يمنع وصول الأكسجين إلى المادة المُحترقة، مما يؤدي إلى إخماد النيران أو الحد من تأجُّجها. وتُعَدُّ صناعة عوامل إخماد الحرائق من الصناعات الكبيرة. ولكن الكثير من مثبطات الحريق التقليدية تكون عبارة عن جزيئاتٍ هالوجينية خطرة على البيئة، وقد تكون ذات تأثيرٍ سامٍّ على الإنسان والحيوان على حدٍّ سواء. إذا ثبتت فاعلية الدي إن إيه في إخماد الحرائق، فسيحظى بأفضلية كونه موجودًا بوفرة وطبيعيَّ التكوين وقابلًا للتحلُّل الحيوي.
من المحتمَل أيضًا استخدام الدي إن إيه في تصميم بطاريات الليثيوم والكبريت، التي تحتوي على مِصْعَدٍ من فلز الليثيوم ومِهْبَط من الكربون والكبريت. عند تشغيل البطارية، تنطلق أيونات الليثيوم من المِصْعَد (الأنود) وتتفاعل مع الكبريت عند المِهْبَط (الكاثود) لتكوين متعدِّدات الكبريتيد. ويُعكَس هذا التفاعل عند إعادة شحن البطارية. ولكن، يُفقَد بعض الكبريت من المِهْبَط عند تشغيل البطارية، مما يُقلل من كفاءتها. تتمتَّع قواعد الأحماض النووية ومجموعات الفوسفات في الدي إن إيه بأُلفة كيميائية قوية مع الكبريت، ويُعتقَد أن تغطية المِهْبَط بالدي إن إيه ربما تحول دون فَقْد عنصر الكبريت على هيئة إلكتروليت.



